Images
Contact

Un treball realitzat pel laboratori de Xavier Salvatella indica que la toxicitat de les fibres amiloides recau en les seves propietats estructurals.
Importants malalties neurodegeneratives com ara el Parkinson i l'Alzheimer estan relacionades amb la formació d’agregats proteics en forma de fibres amiloides. Malgrat la importància que tenen aquests dipòsits, se’n sap ben poc sobre la causa de la toxicitat i el mecanisme pel qual danyen les cèl·lules. Un treball recentment publicat al Journal of Molecular Biology per investigadors de l'Institut de Recerca Biomèdica (IRB Barcelona) i de la Universitat de Cambridge, liderats per Xavier Salvatella i Christopher Dobson, dóna una mica de llum sobre l'origen de la toxicitat.
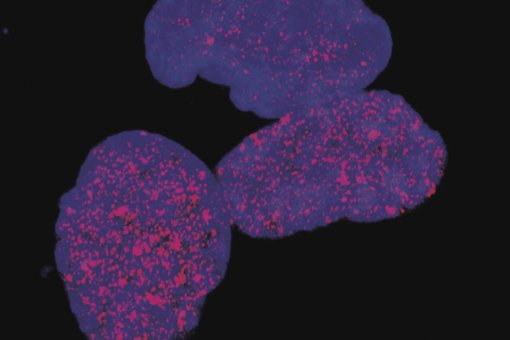
Maria Mossuto, investigadora en el laboratori de Salvatella, ha estudiat les fibres formades per una proteïna anomenada lisozim, que són causants de la amiloïdosi sistèmica no neuropàtica, una malaltia rara. Mossuto ha vist que la mateixa proteïna pot formar almenys dos tipus de fibres diferents. En condicions de formació diferents va obtenir, per una banda, unes fibres molt estables i molt estructurades i, per l’altra, unes menys estables i que contenen una part estructurada i una altra part desordenada. Quan va aplicar aquestes fibres a cultius cel·lulars va veure que les fibres estructurades no son tòxiques per a les cèl·lules, mentre que les fibres parcialment desordenades les perjudiquen fins provocar la mort. Amb aquests resultats, el treball apunta a que la toxicitat no depèn de la mida de l'agregat, sinó de les seves propietats estructurals.
Després d'aquesta troballa, encara queden moltes preguntes per respondre i el treball futur del laboratori de l'IRB Barcelona es centrarà en estudiar com exerceixen les fibres la seva funció tòxica. Per això, tractaran de descobrir si els agregats entren o no en les cèl·lules, si les fibres menys ordenades es trenquen en fragments i actuen llavors com a oligòmers - i per això són tòxiques-, si s’associen amb altres proteïnes que influeixen en la seva activitat, etc. A més volen estudiar si la fracció de proteïna que està aparentment desordenada en les fibres realment ho està, o si es plega parcialment. "La funció i estructura de la proteïna lisozim és coneixen molt bé i treballar amb ella ens permet entendre els principis fonamentals del procés d'agregació. L'objectiu és establir una metodologia que permeti després estudiar altres proteïnes d'especial rellevància clínica ", diu Salvatella.
Article de referència:
The Non-Core Regions of Human Lysozyme Amyloid Fibrils Influence Cytotoxicity.
Mossuto MF, Dhulesia A, Devlin G, Frare E, Kumita JR, de Laureto PP, Dumoulin M, Fontana A, Dobson CM, Salvatella X.
Journal of Molecular Biology (2010) doi:10.1016/j.jmb.2010.07.005
Nahia Barbería
IRB Barcelona
L’Institut de Recerca Biomèdica (IRB Barcelona) treballa per aconseguir una vida lliure de malalties. Desenvolupa una recerca multidisciplinària d’excel·lència per curar el càncer i altres malalties vinculades a l'envelliment. Treballa establint col·laboracions amb la indústria farmacèutica i els principals hospitals per fer arribar els resultats de la recerca a la societat a través de la transferència de tecnologia, i du a terme diferents iniciatives de divulgació científica per mantenir un diàleg obert amb la ciutadania. L’IRB Barcelona és un centre internacional que acull al voltant de 400 investigadors de més de 30 nacionalitats. Reconegut com a Centre d'Excel·lència Severo Ochoa des de 2011, és un centre CERCA i membre del Barcelona Institute of Science and Technology (BIST).